中华医学会器官移植学分会肝移植学组 中国医师协会器官移植医师分会 杨家印,四川大学华西医院肝移植中心、器官移植中心、普通外科,成都 活体肝移植作为解决器官供需矛盾的主要手段之一,在临床实践中常面临移植物体积不足可能导致受者出现小肝综合征的问题;而若移植物占比大,切取后剩余肝脏体积过小,则可能增加供者术后发生肝功能不全甚至肝衰竭风险。为应对这一双重挑战,双供者肝移植技术应运而生。该技术在最大限度减少单个供者肝脏切除体积、保障供者手术安全的同时,能够通过两份移植物为受者提供足够体积的功能性肝组织,从而提高受者术后肝功能恢复的成功率。然而,目前双供者肝移植在我国的临床应用仍较为有限。 为推动该技术在国内的规范化和推广应用,进一步缓解器官短缺问题,中华医学会器官移植学分会肝移植学组、中国医师协会器官移植医师分会组织国内肝移植领域的专家学者,结合国际先进移植中心的成熟经验,并采用牛津循证医学中心证据质量与推荐强度分级标准,从供者及移植物的评估与选择、手术方式的实施到术后并发症的防治等方面,制订《中国双供者肝移植临床实践指南(2025版)》。该指南旨在为临床提供科学、系统的指导,提升我国双供者肝移植的整体水平,为拓展器官供者来源、保障移植安全与疗效提供有力支持。 双供者肝移植;活体器官捐献;公民逝世后器官捐献 一、前言 肝移植是目前治疗终末期肝病最有效的治疗方式之一,然而,供肝短缺是限制其广泛应用的主要瓶颈。公民逝世后器官捐献已成为重要的供肝来源,但仍难以满足日益增长的临床需求[1]。在此背景下,活体肝移植逐渐发展为重要的替代性供者来源。然而,活体肝移植(living donor liver transplantation,LDLT)在应用过程中仍面临诸多挑战,尤其在供者安全、移植物体积不足及受者小肝综合征防治等方面尚需持续优化[2]。 2001年,Lee等[3]首次报道双供者肝移植(dual-graft liver transplantation,DGLT)。2005年,严律南教授及其团队完成了我国DGLT手术[4]。但受限于技术难度、团队经验及管理体系,该技术尚未在全世界范围内广泛推广。 为推动DGLT技术在我国的规范化开展,充分发挥其在缓解供肝短缺中的潜在作用,中华医学会器官移植学分会肝移植学组、中国医师协会器官移植医师分会组织国内相关专家,结合国际先进经验与临床实践,参照牛津循证医学中心(Oxford Centre for Evidence‑Based Medicine,OCEBM)证据质量与推荐强度分级标准,围绕供者与移植物评估、手术技术、术后管理及并发症防治等核心内容,制订《中国双供者肝移植临床实践指南(2025版)》(以下简称本指南)。本指南旨在为临床实践提供科学、规范的指导,提升我国双供者肝移植技术水平,进一步缓解器官供需矛盾,惠及更多终末期肝病患者。 二、指南形成方法 本指南已于国际实践指南注册与透明化平台(Practice guideline REgistration for transPAREncy,PREPARE)完成中英文双语注册(注册号:PREPA RE⁃2025CN763)。 临床问题的遴选及确定:指南专家组首先对国内外相关研究成果进行全面梳理,由执笔专家提出双供者肝移植中亟待解决且具有临床实践意义的问题。通过问卷调查和多轮专家会议讨论,最终确定本指南需解决的6个临床问题,内容涵盖双供者肝移植临床意义、安全性、供受者选择与评估、移植物类型选择、植入方式选择等。 证据检索与筛选:指南编写小组采用人群、干预、对照与结局模型,围绕所确定的临床问题,在PubMed、The Cochrane Library、中国生物医学文献数据库、万方数据、中国知网等权威数据库进行文献检索。检索范围涵盖国内外指南、共识、系统评价、Meta分析、RCT、非随机队列研究及病例对照研究,检索关键词包括“肝移植”“活体肝移植”“双供者肝移植”等。检索时限为1978年1月至2025年1月,纳入文献语言限定为中文和英文。检索后由指南编写小组成员独立进行文献筛选,依次审阅标题、摘要及全文,确定符合纳入标准的文献。若存在分歧,则通过专家组讨论协商或邀请独立专家仲裁达成共识。证据分级和推荐强度分级:本指南使用OCEBM证据质量与推荐强度分级标准(2009版)对每个临床问题的证据质量和推荐强度进行分级(表1)。
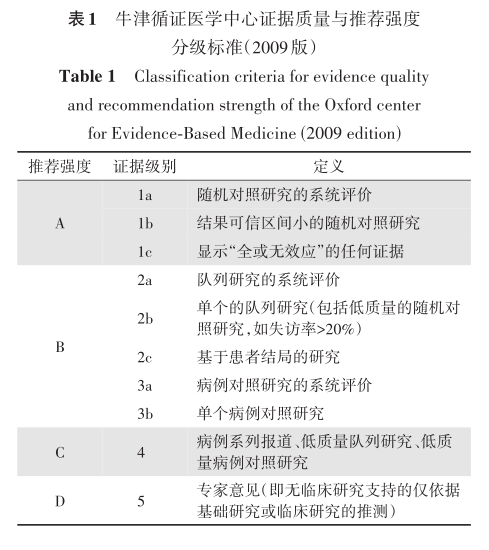
推荐意见的形成:基于循证医学证据,综合考虑我国患者的临床需求、价值观、经济成本及利弊因素,工作组共形成16条临床推荐意见。经中华医学会器官移植学分会和中国医师协会器官移植医师分会组织专家组讨论,并根据反馈意见进行两轮修订后,最终形成该指南。
三、推荐意见及说明
临床问题1:为什么要开展双供者肝移植?
推荐意见1:双供者肝移植能够在保障供者安全的同时,有效避免受者小肝综合征的发生。(推荐强度A,证据等级1c)
推荐意见2:与单一活体供肝移植相比,双供者肝移植可最大限度减少单一供者的捐献肝脏体积,从而降低手术风险,更好地保障供者的安全。(推荐强度B,证据等级2b)
推荐意见说明:
肝移植是治疗终末期肝脏疾病的唯一有效方法,但公民逝世后器官捐献的短缺仍是限制患者获得肝移植的重要因素。LDLT已成为扩大供者来源、缓解供需矛盾的重要手段。在LDLT实践中,供者的安全保障和受者小肝综合征的预防是两大关键挑战[2]。
为确保供者安全并满足受者的代谢需求,通常建议供者术后剩余肝体积不低于术前肝脏总体积的30%~35%,同时受者的移植物质量比(graft-to-recipient weight ratio,GRWR)通常需≥0.8%[5‑9]。然而,受限于供者年龄、肝脏体积、肝脏脂肪变性及其他身体、心理和社会因素,部分情况下单一潜在供者无法单独完成足量肝脏捐献[10‑11]。DGLT在此背景下提供了有效的解决方案。通过将移植物来源分配至两位供者,DGLT可显著降低单一供者的肝切除体积,在保障供者安全的同时,满足受者对足够体积移植物的需求,并扩大了供者选择范围。此外,DGLT的应用还可使部分原本不符合捐献标准的部分临界状态(如轻度脂肪肝、年龄偏大)的活体供者得以利用,进一步拓展供肝来源。
另外,尽管LDLT技术已日趋成熟并广泛应用,但其供者手术风险始终难以完全避免。一旦供者发生严重并发症甚至死亡,将对受者、供者家庭及移植团队带来极大心理与伦理冲击[5,12]。相较之下,DGLT通过分担肝脏切除量既可在一定程度上降低单个供者的手术风险,又能最大限度降低受者术后小肝综合征的发生率,在供、受者安全层面具有伦理合理性。然而,DGLT需两名健康供者同时接受捐献手术,整体捐献风险总量亦随之增加,仍可能带来额外的伦理压力与心理负担。因此,在实施DGLT时,应充分评估供受者双方风险与获益,综合权衡,谨慎决策[13‑15]。
临床问题2:双供者肝移植的供、受者手术安全性
推荐意见3:在具备成熟活体肝移植经验、完善围手术期管理体系及多学科团队支持的移植中心,双供者肝移植活体供肝获取可安全开展,供者围手术期严重并发症发生率低。(推荐强度B,证据等级2b)
推荐意见4:双供者肝移植受者术后在院期间死亡率及总体生存情况与单一供者活体肝移植相比无显著差异。(推荐强度B,证据等级2b)
推荐意见说明:
供者安全始终是DGLT技术应用中需优先关注的核心问题。根据现有文献,在具备成熟经验和完善管理体系的移植中心,DGLT活体供肝获取可安全实施,目前尚无供者死亡事件报道。Song等[7]的多中心研究结果显示:DGLT供者手术总并发症发生率为1.9%,与单供者活体肝移植总并发症发生率无明显差异。其中,需进一步干预的Clavien⁃Dindo Ⅲ级(需手术、内镜或介入治疗)及Ⅳ级(危及生命需重症监护)严重并发症发生率低,仅为1%~3%。在DGLT供者手术中,多采用左半肝或左外叶切除术,其切除肝体积较小、解剖复杂度较低,整体技术难度低于常规LDLT中的右半肝切除术。既往研究结果显示:左叶供肝者的手术风险普遍低于右叶供肝者[16]。因此,在能够独立、安全开展活体肝移植,尤其具备右半肝供肝手术经验的移植中心,其供者手术团队通常已具备完成DGLT活体供肝获取手术的技术能力。
对于受者,DGLT的手术整体技术难度较高,术中操作复杂,移植物血管与胆道重建繁琐,手术时间延长,术中风险增加。然而,现有多项研究结果显示:DGLT受者在院期间死亡率、短期与远期生存率与常规LDLT相当[7‑8],提示在严格供、受者选择与完善团队保障下,DGLT可获得与常规LDLT相当的安全性。
临床问题3:双供者肝移植中供、受者评估与选择
推荐意见5:双供者肝移植应严格遵循活体供肝供者评估原则,确保每例供者经全面检查后符合捐献条件,身体健康且无可能危及受者的传染疾病或手术禁忌证;应通过影像学检查和肝体积测定确认供者术后剩余肝体积至少为原肝体积的30%~35%,以保证供者安全。同时确保肝脏捐献者知晓完整捐献过程并能克服可能出现的心理障碍。(推荐强度B,证据级别2b)
推荐意见6:双供者肝移植适用于单一供者供肝无法满足受者最低安全移植物需求的情况,通常联合供肝GRWR应≥0.8%或总体积达到>40%标准肝体积。(推荐强度B,证据等级2b)
推荐意见7:对于终末期肝病模型(model for end‑stage liver diseas,MELD)评分≥30分或年龄≥60岁的受者,双供者肝移植手术风险显著升高,应谨慎评估适应证。(推荐强度B,证据等级2b)
推荐意见说明:
活体供者安全始终是DGLT的首要原则。供者评估基本参照常规LDLT流程,主要包括以下3个方面目标:
(1)确保安全获取足够体积的供肝。
(2)避免供者来源性疾病传播给受者。
(3)确保供者充分知晓捐献过程并具备良好心理承受能力[5,17-19]。
评估过程中需详细了解供者年龄、健康状况、病史及家族史,并完善血清学及影像学检查(如腹部三维CT、MRCP),全面评估肝脏功能、解剖结构及血管、胆管变异情况[20]。对于存在脂肪肝高危因素(如肥胖、糖尿病、血脂异常)和(或)影像学检查提示脂肪变性的供者,建议术前根据具体情况行肝穿刺活组织病理学检查,以明确大泡性脂肪变性程度[7‑8]。
此外,公民逝世后器官捐献供者亦可作为DGLT供肝来源。此类供者的评估应参考劈离式肝移植的供者筛选标准,除评估解剖结构、肝脏体积及质量外,还应综合考虑死亡原因、ICU住院时间、升压药使用及内环境稳定性等因素[21]。鉴于DGLT通常能够提供充足的移植肝体积,其供肝选择标准可较常规LDLT及劈离式肝移植适度放宽。
DGLT受者的选择应严格把握适应证以最大化手术获益。通常认为,当受者体型较大(如成年男性或高体质量患者),单一供者无法提供最低移植肝需求时,可考虑DGLT[22]。普遍采用的标准为联合供肝GRWR≥0.8%或移植物体积达到≥40%标准肝体积;当低于此阈值时,小肝综合征发生率显著增加,移植预后不良[23‑25]。此外,还应充分评估受者病情严重程度及全身状况。对于MELD评分极高或病情危重者,应慎重考虑DGLT方案。在MELD评分≥30分的高危受者中,DGLT术后90 d内死亡率高达30%,明显高于普通LDLT患者[26]。Song等[7]的研究结果显示:MELD评分≥30分以及受者年龄≥60岁是影响受者预后的独立危险因素。因此,DGLT受者的选择应在确保移植肝体积充足的基础上,平衡整体风险,尤其对高危受者人群仍应持谨慎态度。
临床问题4:双供者肝移植中供肝类型的选择
推荐意见8:双供者肝移植的供肝来源主要包括双活体供肝以及活体供肝联合公民逝世后器官捐献供肝两种模式,其中以双活体供肝模式最为常见。(推荐强度B,证据级别2b)
推荐意见9:活体供肝联合公民逝世后捐献供肝模式有助于在满足受者需求的同时减少活体供者例数以降低供者手术风险,缓解伦理压力;同时简化血管与胆管吻合操作,降低手术技术难度。(推荐强度C,证据级别4)
推荐意见10:双供者肝移植移植肝组合类型应根据供者安全性、移植肝体积需求与受者条件综合确定,常用组合包括左半肝+左半肝、左半肝+左外叶、左外叶+左外叶、右半肝+左半肝、右半肝+左外叶。(推荐强度B,证据级别2b)
推荐意见说明:
按供肝来源分类,目前DGLT的供者来源仍以双活体供者模式为主[13]。尽管DGLT通过联合供肝可在供者安全性方面取得一定平衡,但双活体供者模式依然需要2名健康供者接受肝切除手术,其累积并发症发生率与伦理压力需综合考量。为缓解该问题,严律南教授成功实施我国活体供者联合公民逝世后器官捐献供者的DGLT手术,通过减少1例活体供者,实现了降低供者风险同时保障受者安全的目的[4]。此外,公民逝世后器官捐献肝脏通常具备充足的血管与胆管长度,有助于降低血管与胆管吻合难度。另外,国内樊嘉教授和周俭教授团队报道1例活体供者联合“废弃肝”应用于DGLT的病例。该受者右侧移植物来自亲属捐献的右半肝,左侧移植物则来自1例因肝腺瘤接受肝切除术后自愿捐献的左半肝。该肝移植模式作为活体供肝体积不足时的应急补充策略,为DGLT供肝来源开辟了新的探索方向[27]。近期,国内张宇教授团队亦尝试将因胆管结石而切除并经处理后的“废弃”右半肝用于肝移植,进一步拓展了边缘供肝的临床应用场景[28]。
在移植物组合类型方面,DGLT可灵活采用来源于左肝(左半肝、左外叶)及右肝(右半肝、改良右半肝、扩大右半肝、右后叶)的多种组合模式[3‑4,7‑8,13,26⁃27,29‑34]。考虑到左半肝及左外叶切除技术相对成熟、风险低,且双左肝组合通常可满足受者移植物容量需求,因此,其成为DGLT中最为常用的组合模式[35]。Song等[7]报道在400例双供者活体肝移植中,双左侧供肝的比例达70.5%,其中包括左半肝+左半肝、左半肝+左外叶及左外叶+左外叶组合;而右肝联合左肝的组合占29.5%。
临床问题5:双供者肝移植中移植物植入方式的选择
推荐意见11:双左肝移植物植入时,建议第1个移植物置于左肝解剖位置,第2个移植物左右翻转180°后置于右肝解剖位置,依次完成肝静脉、门静脉、动脉及胆管吻合;右侧胆管吻合先于右侧门静脉吻合。(推荐强度B,证据级别2b)
推荐意见12:右肝联合左肝移植物植入时,建议右肝先置入右肝区完成血管吻合并灌注,再完成左肝移植物置入与血管吻合,最后依次完成右侧胆管端端吻合及左侧Roux‑en‑Y胆肠吻合。(推荐强度B,证据级别2b)
推荐意见13:双左肝移植物左右放置顺序建议综合考虑胆管数量、管径及解剖匹配度,优先将胆管复杂或与受者不匹配的移植物放置于左侧。(推荐强度B,证据级别2b)
推荐意见14:体外拼接技术可作为部分双供者肝移植中的辅助技术,可降低体内吻合难度,缩短无肝期,但需在高水平移植中心谨慎应用。(推荐强度C,证据级别4)
推荐意见说明:
DGLT移植物的植入方式根据移植物的组合决定,双左肝移植物具体手术过程如下:
(1)阻断受者门静脉与下腔静脉,完成病肝切除。
(2)将第1个左侧移植物放入受者原左肝的解剖位置,并将其流出道与受者左肝静脉和中肝静脉开口进行吻合。
(3)将第一移植物的门静脉与受者门静脉的左支进行端端吻合。
(4)阻断受者的右肝静脉断端及门静脉右支断端,然后松开下腔静脉及门静脉阻断钳开始灌注第一移植物。
(5)完成第一移植物的动脉吻合。
(6)将第2个左侧移植物左右翻转180°后,放置于受者原右肝的解剖位置,并将其静脉流出道与右肝静脉的断端进行端端吻合。
(7)由于第二移植物经过左右180°翻转,胆管位于门静脉后方,如果在完成门静脉吻合后再进行胆管吻合会变得困难,因此建议先吻合第二移植物胆管。
(8)吻合第二移植物的门静脉,松开阻断钳,开始灌注第二移植物。
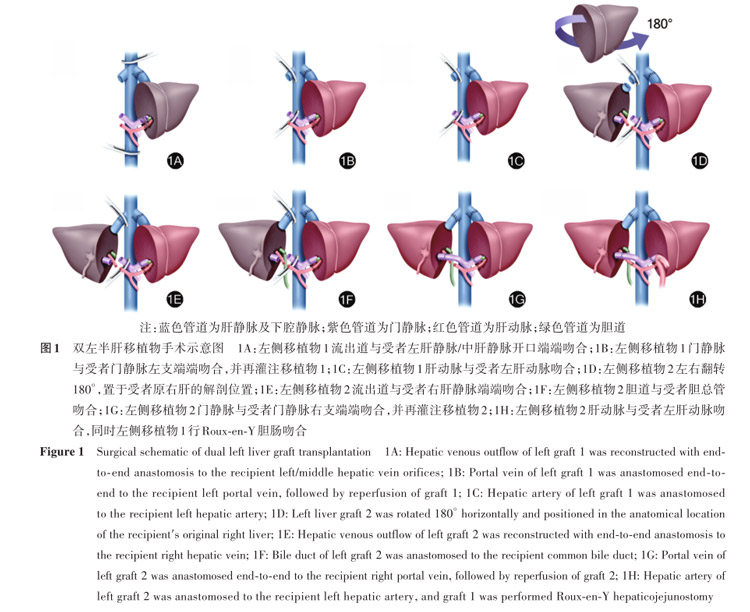
(9)进行第二移植物的动脉及第一移植物胆管的Roux-en‑Y胆肠吻合(图1)。
由于左肝移植物通常较右肝更小,无法完全填充受者右肝窝空间,通常需要放置不同尺寸的组织扩张器来支撑固定右侧移植物,以防止术后因移植肝移位所引起的血管、胆管牵拉,而导致移植肝血管、胆道并发症[4,7,32,36]。双左肝移植物的左右放置位置主要取决于2个移植物的胆管管径和数量。如果将移植物放置于右侧进行胆肠吻合术在技术上不可行,则通常会将具有多个胆管开口或胆管管径与受者胆管不匹配的移植物放置在左侧。如果两个移植物均为单一胆管开口且管径相似,则可以根据移植物或受者肝动脉的数量或长度来决定。如果其他条件相似,通常建议将质量更好的移植物放置在左侧[7]。
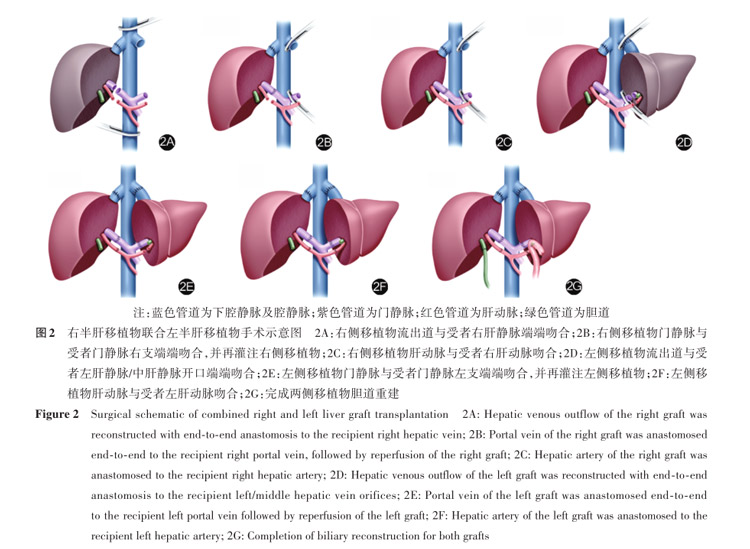
对于右肝移植物联合左肝移植物的DGLT,该移植物组合及置入方式更符合肝脏的正常解剖位置,与常规的活体右半肝和活体左半肝植入过程类似,也相对降低了血管和胆管吻合难度,其不足之处是右侧供肝的获取会增加供者的手术时间和风险,因此,在当前双左侧供肝通常已能满足受者需求、且能缩短手术时间并能提高供者安全性的情况下,右侧供肝联合左侧供肝模式的应用少于双左半肝供肝[35]。
右侧供肝联合左侧供肝的移植物置入具体手术过程为:
(1)阻断受者门静脉与下腔静脉,完成病肝切除。
(2)将右肝移植物放入原右肝的解剖位置,并将移植物的流出道与受者的右肝静脉进行端端吻合,是否重建中肝静脉Ⅴ、Ⅷ段分支的标准与活体右半肝移植一致(如中肝静脉残端长径>5mm,建议重建中肝静脉)。
(3)右侧移植物门静脉与受者门静脉右支进行端端吻合,吻合完成后阻断受者左肝静脉断端,松开下腔静脉阻断,再阻断受者门静脉左支断端,松开右侧门静脉阻断开始灌注右侧移植物。
(4)吻合右侧移植物动脉。
(5)将左侧移植物放入受者左肝解剖位置,将移植物左肝静脉与受者左肝静脉和中肝静脉开口进行吻合。
(6)将左肝移植物门静脉与受者门静脉左支进行吻合,松开所有阻断钳,灌注左侧移植物。
(7)吻合左侧移植物动脉。
(8)根据双侧移植物胆管开口数量以及直径选择合适的胆管吻合方式(图2)[4,7,32,36]。
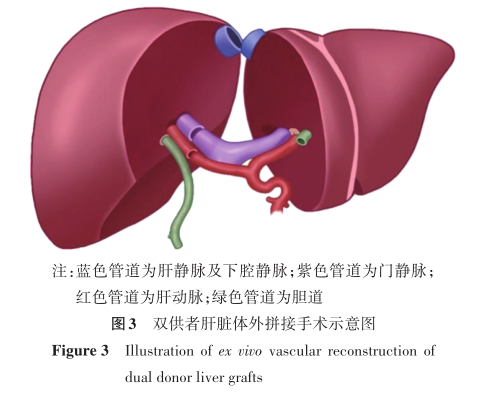
国内杨家印教授团队报道1例采用双供者肝脏体外拼接技术的案例,即将两个移植物在体外完成血管重建后整体植入受者。该手术使用来自活体供者的不含中肝静脉的右半肝(移植物1:含右肝静脉、门静脉右支及右肝动脉)与来自公民逝世后捐献供者的肝左外叶(移植物2:含左肝静脉、门静脉主干、门静脉左支、门静脉右支残端、肝总动脉、肝固有动脉、左肝动脉、右肝动脉残端)进行体外拼接重建。拼接过程中通过来自公民逝世后供者的血管补片,将移植物1的肝右静脉与移植物2的肝左静脉整型成单一的肝静脉流出道。随后,将移植物1的门静脉右支与移植物2的门静脉右支残端行端侧吻合;移植物1的右肝动脉与移植物2的右肝动脉残端进行端端吻合(图3)。最终采用改良背驮式肝移植技术,将整形后的肝静脉流出道与受者下腔静脉吻合,移植物2的门静脉主干与受者门静脉吻合,肝总动脉与受者肝固有动脉吻合。该体外拼接策略的优点在于:通过后台精确重建移植物血管结构,有效降低了体内血管吻合的操作难度,显著缩短了无肝期,对复杂双供者肝移植的开展具有重要参考价值[37]。
临床问题6:双供者肝移植术后单侧移植物萎缩的处理
推荐意见15:双供者肝移植后总体并发症发生率较高,应重点关注胆道并发症、肝静脉回流障碍、门静脉吻合口狭窄、术后出血、胆漏和肝动脉血栓等常见问题。建议术后加强监测,及时干预。(推荐强度B,证据级别2b)
推荐意见16:双供者肝移植后部分受者可能出现单侧移植物萎缩,多见于异位放置及体积较小的移植物,尚无明确有效的治疗措施,但通常不影响受者长期预后。建议通过影像学动态监测移植物体积与血流变化以完成病因评估,指导长期随访管理。(推荐强度C,证据级别4)
推荐意见说明:
在DGLT中,由于涉及双侧移植物的血管与胆管吻合,整体手术复杂性显著高于常规单供肝移植,围手术期并发症发生率亦相对升高。DGLT受者总并发症发生率约为50%,主要并发症包括胆道并发症、肝静脉回流障碍、门静脉吻合口狭窄、术后出血、胆漏及肝动脉血栓等。尽管DGLT并发症发生风险升高,但在具备成熟技术和系统管理经验的移植中心,绝大多数并发症可通过介入、内镜或手术干预有效处理,受者长期生存率可达与常规活体肝移植相当的水平[7]。
在DGLT中,除上述常见并发症外,术后单侧移植物萎缩是需重点关注的特殊并发症。已有研究结果显示:双移植物在体内可能存在功能性相互抑制,导致在术后1~18个月内部分受者出现单侧移植物萎缩,发生率约为16%[13,38]。单侧移植物萎缩多见于异位放置及体积较小的移植物,可能与术后肝内血流分布不均衡相关[39]。通常体积较大的移植物具备更强的再生能力,而在体积差异明显的双移植物间,其肝静脉及门静脉血流分布亦存在显著差异。对于体积较小或出现萎缩的移植物,通常伴随肝静脉流出道阻力增加及门静脉血流逐渐减少,陷入“低灌注‑萎缩”的恶性循环[40‑41]。但目前未发现单侧移植物萎缩会显著影响总体移植物功能及受者长期预后[13,39]。由于目前相关病例报道有限,移植物萎缩的具体病理生理机制仍有待进一步研究。术后应加强移植物血流动力学系统监测、移植物与宿主免疫学相互作用评估及长期随访管理[13,42]。
DGLT作为活体肝移植的重要技术补充,能够在严格保障供者安全的同时,为受者提供足够的肝脏体积,有效避免小肝综合征的发生,拓展了供者来源,具有显著的临床意义与伦理价值。近年来,随着手术技术的不断进步与多学科团队协作水平的提升,DGLT在手术方式选择、供受者评估、体外拼接等方面积累了宝贵的经验,逐步形成了一套相对成熟的临床策略体系。
展望未来,DGLT作为一种技术难度高、资源协调要求高的复杂手术方式,其进一步发展仍面临诸多挑战。当前仍需开展更大样本量、多中心、长期随访的前瞻性研究,以进一步验证DGLT在不同受者人群中的安全性与有效性;同时,需加强对单侧移植物萎缩、移植物间血流动力学相互作用等内在机制的深入研究,推动影像学与功能学评估手段的标准化。
由于供器官短缺问题的长期存在及临床需求的持续增长,DGLT有望成为终末期肝病患者的重要救治选项。未来,借助AI、影像导航、个体化评估等新兴技术的赋能,双供者肝移植将不断优化决策路径,提高手术安全性与长期疗效,迈入更加精准、高效与可持续的发展阶段。
内容来源:中华消化外科杂志
文本加工:肝癌在线

 简体中文
简体中文
 ENGLISH
ENGLISH

